|
|
Soit une transformation AB + CD à AC + BD.
Recherchons la valeur de l'enthalpie de réaction standard associée à cette transformation :
Si les corps simples sous leur forme moléculaire la plus simple ont pour formule chimique A2, B2, C2 et D2, l'application de la loi de Hess au cycle ci-dessous :
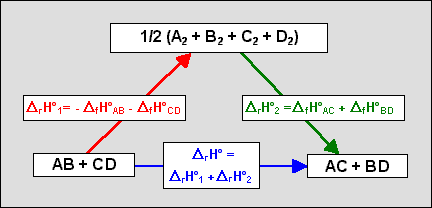
conduit à la relation générale :
Il suffit donc de disposer des tables d'enthalpie de formation à 298K pour calculer la variation d' enthalpie associée à n'importe qu'elle réaction chimique à cette même température.
Notez que l'utilisation de la notation Si ni Xi = 0 pour écrire la réaction chimique permet de simplifier la relation ci dessus puisque cette dernière s'écrit alors :
|
Une réaction chimique est tirée au sort : vous devez alors utiliser les tables d'enthalpies standard de formation pour calculer l'enthalpie standard de réaction. |
Cet exercice vous permet de comparer la précision avec laquelle on obtient une enthalpie standard de réaction, soit à partir de tables d'enthalpie standard soit à partir de tables d'énergies de liaison. |